奥氟格列隆,会成为降糖降重的下一代王者吗?
今年2月,礼来公布了小分子GLP1奥氟格列隆的ACHIEVE-3三期临床结果,结果显示,和口服司美格鲁肽相比,奥氟格列隆(36mg)使 HbA1c(糖化血红蛋白)降低了 2.2%,显著优于口服司美格鲁肽的 1.4%。
这一结果,给司美替鲁肽当头一棒,同时,也让业界对奥氟格列隆有更高的期待。
今天,这篇文章,我利用AI,结合摩熵医药数据库,带大家简单了解这个GLP1的未来之星。
奥氟格列隆(Orforglipron,研发代号:LY3502970)是礼来(Eli Lilly)公司开发的一种具有里程碑意义的口服、非肽类、小分子 GLP-1 受体激动剂。
它被认为是继注射用 GLP-1(如司美格鲁肽)之后的下一代“颠覆性”减重与降糖药物。
1. 研发历史:从小分子到口服突破
奥氟格列隆最初是 Chugai Pharmaceutical(中外制药)开发,
2018年礼来公司以5000万美元的预付款,从中外制药获得了Orforglipron(当时已更名为LY3502970)在全球范围内的独家开发和商业化权益。
2. 作用机制:非肽类小分子的“特技”
奥氟格列隆与天然 GLP-1 激素的生物学效应相同,但分子结构完全不同:
激动受体: 它通过与胰高血糖素样肽-1 受体(GLP-1R)结合,模拟 GLP-1 的作用。
分子特性: 它是非肽类小分子,这意味着它对胃酸和蛋白酶不敏感。
变构调节: 相比于多肽,它能更精确地结合受体的跨膜结构域。
代谢效应:
胰腺: 以血糖依赖性方式促进胰岛素分泌,减少胰高血糖素。
大脑: 作用于下丘脑,通过增强饱腹感和抑制食欲来减少热量摄入。
胃部: 延缓胃排空,减缓餐后血糖波动。
3. 临床试验进展:ATTAIN 与 ACHIEVE 系列
礼来启动了两大全球 3 期临床项目,分别针对减重和糖尿病:

4. 临床试验核心结果 (Phase 3)
2025 年底至 2026 年初公布的数据显示,奥氟格列隆在疗效上显著优于现有口服方案:
减重效果 (ATTAIN-1/2):
在非糖尿病的肥胖成年人中,使用 72 周后,最高剂量组的平均减重百分比达到了 14.7% 至 17% 左右。
在伴有 2 型糖尿病的肥胖人群中,减重约 10.5%。
降糖与对比试验 (ACHIEVE-3):
头对头对比: 在针对 2 型糖尿病的 ACHIEVE-3 试验中,奥氟格列隆与口服司美格鲁肽 (14mg) 进行直接对比。
结果: 奥氟格列隆(36mg)使 HbA1c(糖化血红蛋白)降低了 2.2%,显著优于口服司美格鲁肽的 1.4%。
服用便利性: 临床证实其吸收不受进食或饮水限制,这是相比口服司美格鲁肽巨大的临床优势。
安全性: 最常见的副作用为胃肠道反应(恶心、呕吐、腹泻),多数为轻中度,且通常在剂量爬坡期后缓解。
5.疗效数据对比
由于奥氟格列隆是口服小分子,而另外两者主要是注射类多肽,它们的对比可以从给药便捷性和疗效上限两个维度来看。以下是基于 2026 年最新临床数据(包括 ACHIEVE-3 头对头试验)的对比分析:
奥氟格列隆 VS 司美格鲁肽 VS 替尔泊肽
核心疗效对比:减重与降糖,这三者呈现出明显的阶梯式分布:
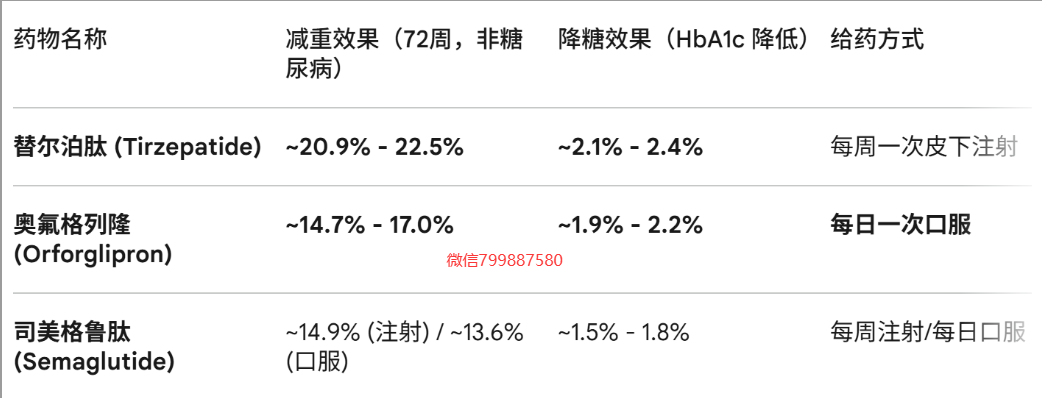
减重: 替尔泊肽(双靶点)依然是目前的“减重天花板”;
奥氟格列隆减重效能已经持平或略微超越了司美格鲁肽的注射版(2.4mg)。
降糖: 在 ACHIEVE-3 头对头试验中,奥氟格列隆(36mg)的表现显著优于目前最强的口服司美格鲁肽(14mg),HbA1c 额外多降低了约 0.7%~0.8%
奥氟格列隆VS司美格鲁肽(口服版)
这是目前医药界最直接的对标,奥氟格列隆在用户体验上完胜:
服用限制:
司美格鲁肽片: 要求非常严苛。必须每天早晨空腹服用,且只能喝不超过 120ml 的白水,服药后必须等待 30 分钟才能进食。
奥氟格列隆:无任何限制,可以随餐服用,不需要控水,这极大提高了长期服用的依从性。
吸收率:
奥氟格列隆是小分子,肠道吸收率稳定且高效;而司美格鲁肽由于是多肽,吸收率极不稳定,极易受到胃部环境影响。
针对“注射恐惧”者的替代方案
奥氟格列隆的出现,实际上填补了替尔泊肽和普通减肥药之间的巨大空白。
对于追求极致减重的人: 替尔泊肽(注射)依然是首选。
对于追求方便、无法接受打针的人: 奥氟格列隆提供了接近注射级别的强劲疗效,彻底终结了“口服药效果差”的历史。
安全性与副作用对比
三者具有高度相似的 GLP-1 类副作用谱:
共同点: 主要为恶心、呕吐、腹泻,且主要发生在加量期(前 8-12 周)。
差异点: 根据最新数据,奥氟格列隆在达到高浓度水平时,胃肠道反应的频率略高于司美格鲁肽。
心率影响: 奥氟格列隆在临床试验中观察到静息心率平均上升幅度略高于另外两者(约增加 2~5 次/分),但目前未发现严重的临床相关心血管风险。
6. 全球注册申报进展
奥氟格列隆正处于全球商业化落地的“最后一公里”:
美国 (FDA): 礼来已于 2025 年提交了减重适应症的上市申请(NDA)。根据 CEO David Ricks 在 2026 年 1 月的表态,由于使用了国家优先审评券,预计 FDA 将在 2026 年第二季度(预计 4 月 10 日前) 做出审批决定。
中国 (NMPA): 礼来于 2026 年初向中国国家药监局提交了上市申请。
考虑到 GLP-1 药物在中国的强劲需求和临床紧迫性,预计最快有望在 2026 年底或 2027 年初获批。
产能准备: 礼来在 2026 年 3 月宣布投资 30 亿美元 在中国扩大生产基地,重点建设“口服固体制剂”供应链,专门支持奥氟格列隆的全球及本土供应。
总结:
奥氟格列隆是目前全球研发进度最快、数据最扎实的小分子口服 GLP-1。它不仅在疗效上超越了现有的口服多肽药物,更通过解决“冷链运输”和“复杂服用限制”的问题,极大地提高了患者的依从性。