首个上市GLP-1小分子奥氟格列隆信息总览
2026年4月1日,礼来GLP-1口服小分子奥氟格列隆(Orforglipron,商品名FOUNDAYO)获FDA批准上市,适应症为用于成人肥胖症(BMI≥30 kg/m²),或至少伴有1种体重相关疾病(如高血压、2型糖尿病等)的超重成人(BMI≥27 kg/m²)的长期体重管理。需配合低热量饮食和增加体力活动。
1.关键里程碑
2018年,礼来从日本中外制药获得orforglipron的全球权益,前期仅支付5000万美元授权费。
ATTAIN临床试验系列(尤其是ATTAIN-1 III期试验):最高剂量下,患者在72周内平均减重约27磅(约12.4%),并在腰围、血脂、血压等心血管风险指标上有显著改善。试验数据为FDA批准提供了核心循证支持。
FDA“局长国家优先凭证”( CNPV)试点计划下首个获批的新分子实体(NME)。从递交申请到获批仅50天,远早于原PDUFA目标日期(2027年1月20日)294天,创下2002年以来NME最快审批纪录。
2.原料药信息
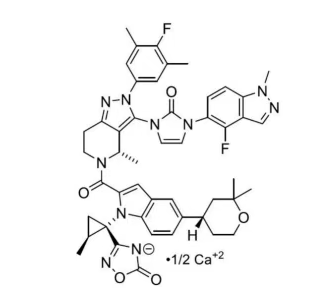
活性成分:奥福格利普隆(orforglipron),以奥福格利普隆钙(orforglipron calcium)盐形式存在。
分子式:C48H47F2N10O5·[0.5]Ca
分子量:902.0
为白色至浅棕色固体,不溶于水,具有引湿性。
3.处方
核心片:共聚维酮、交联聚维酮、硬脂酸镁、微晶纤维素、无水碳酸钠。
薄膜包衣:聚乙二醇、聚乙烯醇、滑石粉、二氧化钛。
不同规格额外着色剂:
0.8mg和9mg:含氧化铁红和氧化铁黄。
2.5mg和14.5mg:含氧化铁黄。
5.5mg和17.2mg:含亚铁氧化铁和氧化铁红。
每片含钠量≤10 mg。
4.规格
片剂(口服,薄膜衣片):
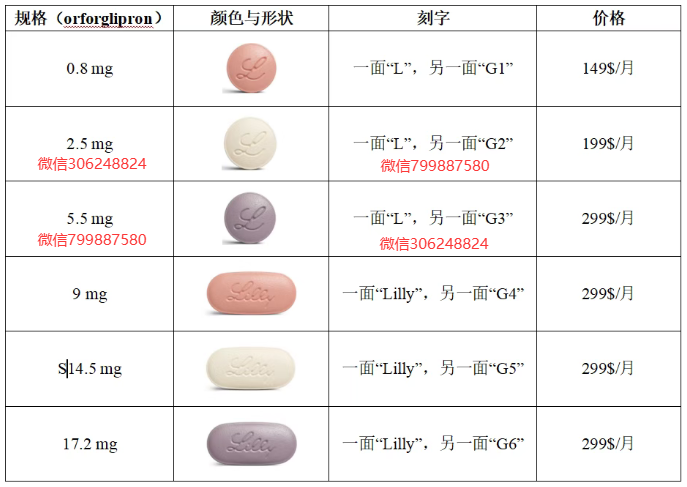
包装:30片/瓶(带干燥剂),瓶装。
5.用法用量
给药方式:口服,每日1次,可与食物同服或空腹。
吞服要求:整片吞服,不可掰开、压碎或咀嚼。
剂量递增方案(为降低胃肠道不良反应风险):
起始:0.8 mg 每日1次,至少30天;
随后:2.5 mg 每日1次,至少30天;
随后:5.5 mg 每日1次;
之后根据疗效和耐受性,每至少30天可递增至下一剂量(9 mg → 14.5 mg → 17.2 mg)。
最大剂量:17.2 mg 每日1次。
漏服处理:尽快补服,不可加倍;若连续漏服≥7天,重新从低剂量开始递增。
特殊情况:与强CYP3A4抑制剂合用时,最大剂量限为9 mg/日;避免与强CYP3A4诱导剂合用。
6.生物利用度
绝对生物利用度:0.8 mg剂量时几何平均值为77%。
食物影响:无临床相关影响(多剂量研究显示,进食状态下AUC₀₋₂₄ₕ降低19%、Cₘₐₓ降低26%,但tₘₐₓ和t₁/₂不变)。
7.PK
口服后Tₘₐₓ为4~8h,暴露量呈剂量正比。半衰期29-49h。
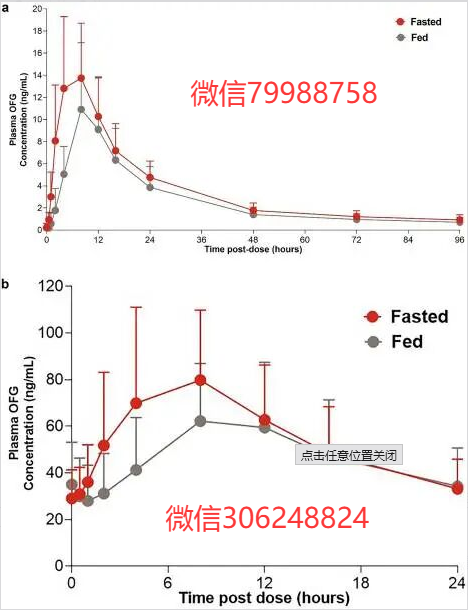
研究a中对健康受试者进行单次口服后,Orforglipron(3 mg)血浆浓度曲线。研究b中,健康参与者多次口服后,Orforglipron(16 mg)血浆浓度分布
8.贮藏
室温20°C~25°C保存;允许短暂 excursions 至15°C~30°C